
Точечный удар по болезни
Аптамеры — это синтетические молекулы, которые можно «научить» избирательно связываться с любыми биологическими мишенями: от вирусов до раковых клеток. Они могут буквально находить опухоль по биомолекулярному «запаху». К аптамеру можно легко прикрепить флуоресцентную метку, лекарство или наночастицу, превратив его в универсальный инструмент для медицины.
Когда аптамер находит свою цель, он либо высвобождает лекарство прямо в пораженную клетку, либо остается на ее поверхности, позволяя активировать терапию внешним воздействием — например, магнитным полем. Это позволяет избежать повреждения здоровых тканей, резко снизить побочные эффекты по сравнению с традиционной химиотерапией и преодолеть устойчивость опухоли к лечению.

По словам доктора физико-математических наук, старшего научного сотрудника Института физики им. Л.В. Киренского СО РАН Феликса Томилина, аптамерные системы доставки позволяют преодолеть главные ограничения современной фармакотерапии: уменьшить дозу препарата, снизить частоту побочных реакций и повысить эффективность лечения. Особенно это перспективно в онкологии.
«Например, классический химиопрепарат цисплатин вызывает серьёзные побочные эффекты. Но если поместить его в „контейнер“ с аптамером, нацеленным на опухоль, дозу можно снизить в 15–20 раз, а токсичность — минимизировать», — уточняет ученый.
Наноскальпель для хирурга
Применение аптамерам нашли и в хирургии, например, в сложных операциях на мозге. Клетки одного из самого агрессивного типа опухолей, глиобластомы, глубоко прорастают в здоровые ткани, образуя невидимые «щупальца», из-за чего хирургу трудно увидеть четкие границы новообразования.
Для таких операций в Красноярске разработали аптамеры, несущие флуоресцентную метку. Их наносят на ткани мозга, после чего аптамеры связываются с опухолью. При подсветке специальным лазером раковые клетки начинают светиться, и хирург видит их четкие границы, что позволяет удалить пораженные участки, не повредив здоровые.

Но даже после этого могут остаться единичные злокачественные клетки. Для борьбы с ними ученые создали «наноскальпель» — магнитные нанодиски. Те же аптамеры, как проводники, подводят их к остаткам опухоли. При включении переменного магнитного поля нанодиски начинают вибрировать, как микроскопические лезвия, механически разрушая раковые клетки. Такой подход позволяет добраться до «невидимых» остатков опухоли и снижает риск рецидива.
Диагностика за полчаса
Аптамеры могут произвести революцию в диагностике. Сейчас для выявления рака или инфекций требуются сложные анализы и дорогостоящее оборудование. Аптамеры позволяют заменить их дешевыми и компактными тест-системами.
В Красноярске уже разработан чип на основе аптамеров, который способен всего за 30 минут выявить в капле крови циркулирующие опухолевые клетки. Это помогает врачам отслеживать состояние пациента и вовремя корректировать лечение. Такие чипы не только быстрые, но и экономичные: их можно использовать многократно, а стоимость производства значительно ниже, чем у современных аналогов.
Кроме того, аптамерные маркеры намного точнее тех, что используются сегодня, например, при ПЭТ-сканировании. Традиционные маркеры (фтордезоксиглюкоза) накапливается не только в опухолях, но и в здоровых активных тканях (мозге, мышцах), что снижает точность диагностики. Аптамеры же действуют прицельно, обеспечивая четкую визуализацию даже микроскопических метастазов.
«Будучи синтетическими аналогами ДНК, аптамеры биосовместимы и легко выводятся из организма. Это делает их идеальными кандидатами не только для диагностики, но и для терапевтического применения, например, в качестве ингибиторов тромбообразования, где они точечно блокируют ключевые этапы биохимических реакций, приводящих к свертыванию крови. Аптамеры могут стать ключевым инструментом в медицине, биотехнологиях, фармацевтике», — отмечает Феликс Томилин.
Путь в клиники
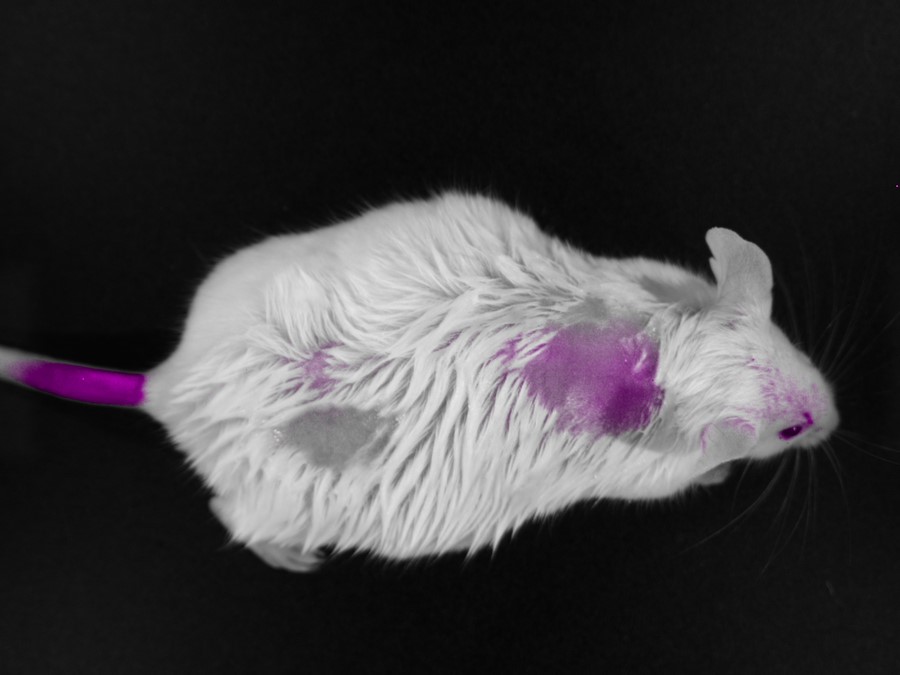
Аптамеры уже доказали свою эффективность в лабораторных условиях: они работают на мышах и кроликах, помогают хирургам и ускоряют диагностику. Но между успехом в лаборатории и реальной медициной стоит барьер — внедрение. Как отмечает Феликс Томилин, технологии готовы к выходу в клиники, но для этого нужны производственные мощности, согласования с регуляторами и сотрудничество с медицинскими центрами.
Создание нового научно-производственного кампуса в Красноярске как раз и призвано решить эту задачу — построить мост между наукой и практикой. Без поддержки на федеральном уровне прорывные разработки рискуют остаться в стенах институтов или уйти за рубеж, где спрос на такие технологии уже сформирован.
Если этот барьер удастся преодолеть, то «умные молекулы», созданные в Красноярске, в ближайшем будущем смогут стать привычным инструментом в больницах по всей стране, спасая тысячи жизней.
Материал подготовлен при поддержке Минобрнауки России в рамках Десятилетия науки и технологий, фото предоставлено КНЦ СО РАН.